【摘要】 深入解析《模拟计算指南》3.6章节——分子的极性与静电性质,涵盖偶极矩、色谱分离机制、溶剂极性本质及log P预测。获刘智攀、赵纪军等专家力荐,提供计算化学实战指南与首样优惠。

关于本书
《模拟计算指南》是唯理计算工程师团队沉淀7年实战经验、历时一年打造,是一本计算化学快速入门指南、材料模拟计算领域的实用宝典。
“书中详细介绍了从理论计算化学的基本原理到目前国际前沿应用体系的计算模拟思路和方法,有利于读者从多维度理解如何采用理论计算方法来解决复杂科学问题,并帮助初学者从中找到适合自己科研的理论支持和计算解决方案。”
——教育部长江学者、杰青、复旦大学教授
刘智攀
“本书以其实用性和易学性为特色,无论是计算物质科学的初学者还是资深研究者,都能从中获得独特的视角和丰富的知识资源,使其成为该领域内一本极具价值的入门及参考书籍。”
——教育部长江学者特聘教授、华南师范大学教授
赵纪军

↑扫码了解更多书籍及唯理计算信息
01文章介绍
今天我们介绍下《模拟计算指南》的3.6分子的极性与静电性质。
习惯上,人们经常讨论某分子的极性是大是小。“极性”在不同场合有多种含义。在色谱分离中,人们通常用极性来解释物质在色谱柱上的保留时间;在选取溶剂时,人们常考虑某溶剂的极性大小。它们往往对应于不同的性质,因此讨论极性时首先要明确其含义和本质。
字面含义上,极性指的是分子中电荷分离的程度。当将分子简单地视作具有一个正电中心和一个负电中心时,可将其看作两个点电荷构成的偶极子,从而可通过偶极矩来加以描述。对于一组偶极子,偶极矩定义为电荷量大小与两个点电荷距离的乘积,是一个数值。更进一步地,还可以定义四极、八极等,其形式是张量。值得注意的是,通常只有当整个分子不带电时才会讨论偶极矩;对于带电分子,总电荷是贡献分子与其他物质之间静电作用的最主要因素,此时分子内部的偶极分布通常不再重要。类似地,通常只有对没有偶极矩的分子,才会讨论四极等高阶项。在量子化学计算中,大多数计算任务都会顺带着输出分子的偶极矩,但如果想要将偶极矩算准,则对计算水平的要求较高,通常要求基组中包含较多的弥散函数(如aug-cc-pVTZ 基组等),因此耗时比普通的单点计算明显更多。
在色谱柱上,某物质的保留时间取决于该分子与色谱柱的相互作用,在色谱柱上吸附较强者将具有更长的保留时间。在很多情况下,分子与色谱柱的结合受静电作用影响明显,人们常常发现同类分子中偶极矩较大者在正相色谱中保留时间较长、在反相色谱中保留时间较短,这是由于分子整体作为偶极子与色谱柱的相互作用在总相互作用中贡献明显。然而仅用偶极矩来描述分子与色谱柱的结合显然是不够的;在大多数情况下,分子内官能团与色谱柱的直接结合对于其相互作用产生了决定性的贡献。对苯二酚结构对称,偶极矩为0,但显然会在正相色谱中表现出相当大的极性,正说明了色谱语境中“极性”的复杂性。在色谱中,两个分子的保留时间长短往往只能通过经验判断;如果要进行计算研究,偶极矩固然可供参考,但更重要的是通过分子与色谱填料的相互作用能量等方式来研究。
对于溶剂的极性,我们通常指的是溶剂通过静电作用稳定其中带电物种的能力,这主要体现在溶剂的介电常数上。高极性溶剂往往具有较大的介电常数,同时可能有较大的偶极矩、可极化性或明显的酸碱性等,但其中介电常数是最主要的。想要得到溶液的介电常数,需要借助分子动力学模拟的手段。
由此可见,上述实际语境下关于“极性”的讨论非常复杂,含义众多,无法使用统一的量加以描述,但有时快速得到一些能一定程度上反映这些“宏观极性”大小的量是有意义的。其中比较重要的是水/辛醇分配系数log P,其定义为化合物在水/辛醇萃取体系中达到平衡时在辛醇中与在水中浓度之比的对数。借助Chemdraw,可以很容易地预测一个化合物的log P,绘制出结构后,点击 View→Show Chemical Properties Window,即可看到基于 Chemdraw内置的经验规则而预测的化合物常见属性。以图3.20中的苯为例,显示log P为2.03,意味着在辛醇中的平衡浓度是在水中的100倍有余,显然苯是十分亲脂的非极性分子。
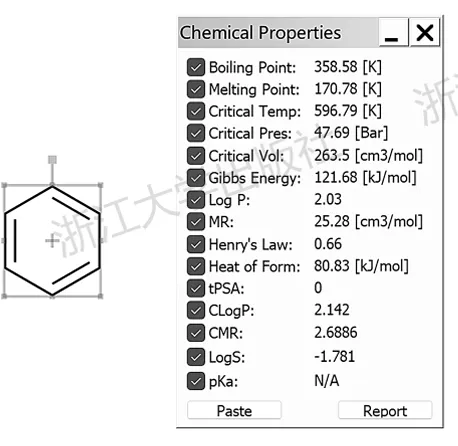
图3 .20 Chemdraw 中预测的苯的各种属性

多位专家力荐 超全实战指南


↑扫码了解更多书籍及唯理计算信息











 您已经拒绝加入团体
您已经拒绝加入团体

 2025-06-17
2025-06-17
 4135
4135
 0
0










