【摘要】 《模拟计算指南》权威解读化学键研究:从原子距离、Mayer键级到ELF分析,揭秘共价键存在性判定方法。结合DFT计算实战案例,展示CuGa₂晶面键合动态与锂化机制。复旦大学、华南师范大学权威专家力荐,助你快速掌握计算化学核心工具!

关于本书
《模拟计算指南》是唯理计算工程师团队沉淀7年实战经验、历时一年打造,是一本计算化学快速入门指南、材料模拟计算领域的实用宝典。
“书中详细介绍了从理论计算化学的基本原理到目前国际前沿应用体系的计算模拟思路和方法,有利于读者从多维度理解如何采用理论计算方法来解决复杂科学问题,并帮助初学者从中找到适合自己科研的理论支持和计算解决方案。”
——教育部长江学者、杰青、复旦大学教授
刘智攀
“本书以其实用性和易学性为特色,无论是计算物质科学的初学者还是资深研究者,都能从中获得独特的视角和丰富的知识资源,使其成为该领域内一本极具价值的入门及参考书籍。”
——教育部长江学者特聘教授、华南师范大学教授
赵纪军

↑扫码了解更多书籍及唯理计算信息
01文章介绍
今天我们介绍下《模拟计算指南》的3.5.1共价键存在性。
对化学键的研究是化学家很重要的任务,其中需要探明化学键的种类、强度、相互作用的本质,及其所带来的反应性。其中,共价键又是重中之重。本节介绍量子化学计算对于共价键的研究手段。
探讨一根化学键时,首先需要判断化学键是否存在。为了判断化学键的存在性可以使用如下方法。
1.将原子距离与典型键长进行比较
当两者距离与两原子共价半径之和接近或更小时,可以认为存在化学键。通过与两原子间各种化学键的典型距离范围比较,可以进一步推断成的是单键、双键等。
必须注意,绝不能用可视化程序自动识别和显示出来的成键来代替人为判断的过程!可视化程序通过某些一刀切的办法自动对原子进行连接而加以显示,时常出现错误,绝不能盲目相信。在绘制分子结构图形时,应当尽可能将成键方式调整正确后再加以展示。
2.计算两原子之间的键级
键级最原始的定义是两个原子间共享的电子对数。在定性分子轨道理论中,画出轨道 能级图并填充电子后,即可统计出两个原子间成键/反键轨道分别填充多少电子,取(成键电子数量-反键电子数量)/2,可得到键级。用这种方法定义的键级显然是0.5的倍数。
这种定义方便直观,但终究是定性的。想要得到准确的键级,仍需借助量子化学计算的手段。正如化学键的强度随着体系不同而连续变化,实际计算得到的键级也是连续的实数。当键级从0开始逐渐增大时,首先对应存在微弱的非键相互作用,随着键级进一步增大,逐渐向着有一定成键、完全的单键、介于单双键之间、典型的多重键等方向连续过渡。
量子化学计算得到的键级有不同的定义方式,其中最常用的是Mayer键级。
3. 计算ELF
ELF(electron localization function,电子局域化函数)是衡量电子聚集程度的指标。对于空间中的任意一点,都可以定义ELF 。ELF总是正实数,其数值越大,表明电子在这一点 处越倾向于聚集。对于绝大多数共价键(反例是charge-shift bond),电子都会聚集在两原子之间的区域,因此观察 ELF 是否在原子间存在明显取到较大数值的区域,是判断共价键存在性的方法之一。
4.观察电子密度差
或许有人会问,既然电子倾向于聚集在成键区域,直接观察电子密度的空间分布是否可行?答案是否定的。这是由于虽然电子会在成键区域相对集中,但最主要仍然分布在原子核附近,如果直接观察电子密度,会发现其分布情况如同是给整个分子蒙上了一层均一的外皮,难以观察到在成键区域的分布细节。因此,电子密度本身对于讨论分子性质几乎没有价值。氯离子与氰化氢形成的氢键复合物的电子密度等值面如图3.13所示,可见非常难以辨认。
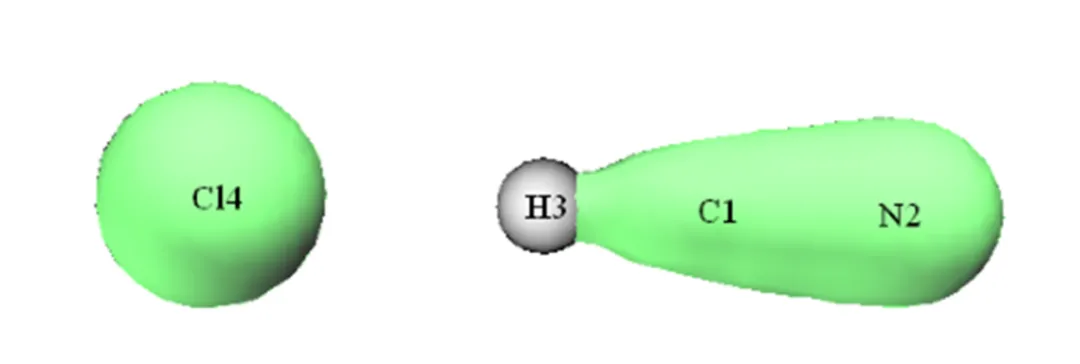
图3.13 氯离子-氰化氢复合物的电子密度等值面
02实战示例
基于上面所讲内容,我们一起看一下文献中的ELF相关计算内容。
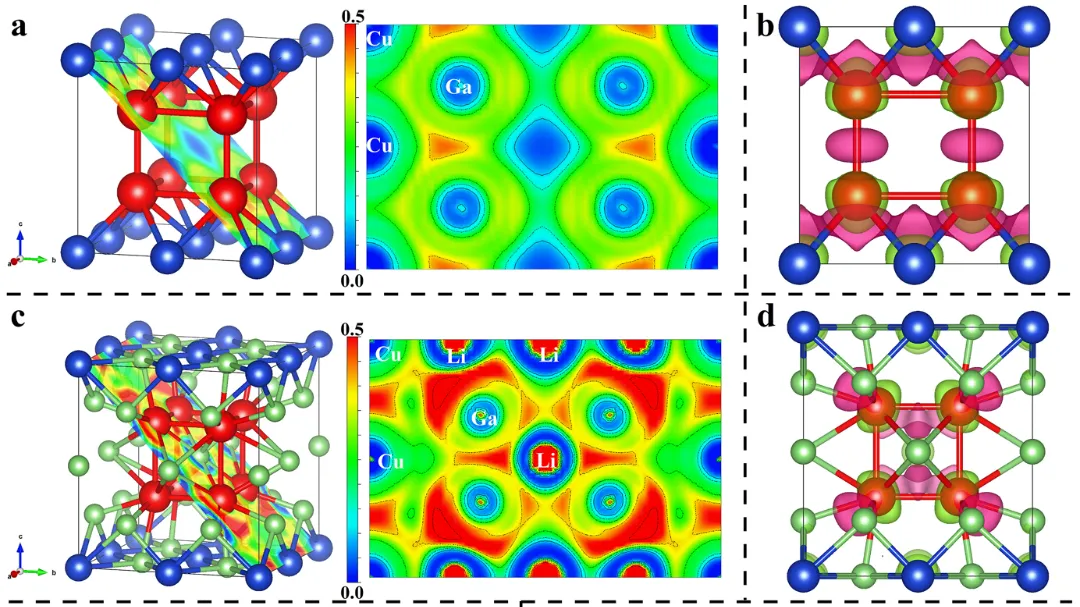
图5
a) CuGa 2(011) 晶面的电子局域化函数。
b) CuGa 2(011) 晶面的变形电荷密度(紫色表示电子密度增加,绿色表示电子密度降低,等密度表面 0.005)。
c) CuGa 2 插入锂原子的电子局域化函数。
d) 插入锂原子后 (011) 晶面后 CuGa 2(011) 晶面的变形电荷密度。
为了揭示 CuGa2过渡层优异性能的潜在机制,进行了DFT计算和ELF分析(图 5)。ELF证明了CuGa2模型中 Cu 和 Ga 之间存在金属键(图 5a金黄色区域)。然而,Li大量嵌入后Cu 和 Ga 之间的金属键被 Li 原子打破。Li 与 Ga 键合行为导致电荷密度重新分布,且优先分布于Li-Ga键周围(图 5c),Cu-Ga在沿着键轴方向上Cu一侧出现更多绿色区域,意味着Cu-Ga键存在一定程度削弱。从差分电荷密度中也能明确观察到Li-Ga键的键合情况以及电荷转移方向。CuGa2中的Cu-Ga 和Ga-Ga,尤其是后者,显示出较强的电子局域特性(图 5b)。在掺杂 Li 原子后Ga-Ga之间相互作用有所增强且在 Cu-Cu 之间观察到CuGa2里面不存在的电子局域现象(图 5d)。
文章中ELF计算的内容总结:
1. 电子局域化函数(ELF)分析:
-
CuGa2的(011)晶面中,Cu与Ga之间存在较强的金属键(图5a)。
-
当Li原子插入CuGa2晶格后(图5c),由于Cu-Ga距离变大,Cu-Ga键的电荷转移被削弱,而Li与Ga之间形成新的键合,导致电子重新分布。
-
变形电荷密度分析(图5b、d)进一步显示,锂化后Ga-Li区域出现强电子局域化,而Cu-Ga键的电子密度降低,说明锂化过程会破坏Cu-Ga键的强度。
-
结合COHP(晶体轨道哈密顿布居)和PDOS(投影态密度)分析,CuGa₂中Cu-Ga键的强结合(ICOHP = -0.119 eV)在锂化后显著减弱(ICOHP = -0.021 eV),证实了Li插入对键合结构的动态影响。
2. 机制解释:
-
锂化时,Li与Ga结合形成LiₓGa合金,削弱CuGa2的金属键,但脱锂过程中Cu与Ga重新结合形成CuGa2,并通过金属键锚定液态金属,防止电极材料脱落。
-
DFT计算揭示了CuGa2对液态镓的锚定机制及锂化反应的动态过程,为实验观察到的优异循环稳定性提供了理论支持。
文献来源:https://doi.org/10.1016/j.est.2024.111879

多位专家力荐 超全实战指南


↑扫码了解更多书籍及唯理计算信息











 您已经拒绝加入团体
您已经拒绝加入团体

 2025-05-27
2025-05-27
 5088
5088
 0
0










