【摘要】 深度解析蛋白质组学如何通过检测蛋白质表达、翻译后修饰等动态变化,解决基因检测在肿瘤靶向治疗中的盲区。涵盖临床转化案例、技术突破及未来发展趋势,为精准医疗提供多组学解决方案。
2003年人类基因组计划的完成,揭开了基因组医学的新纪元。但在癌症临床实践中,单纯依赖基因检测的局限逐渐显现——约60%的肺癌患者无法通过基因突变找到有效靶点。此时,蛋白质组学以"分子显微镜"的姿态,为肿瘤精准治疗增添了关键维度。
一、蛋白质组学如何突破基因检测瓶颈
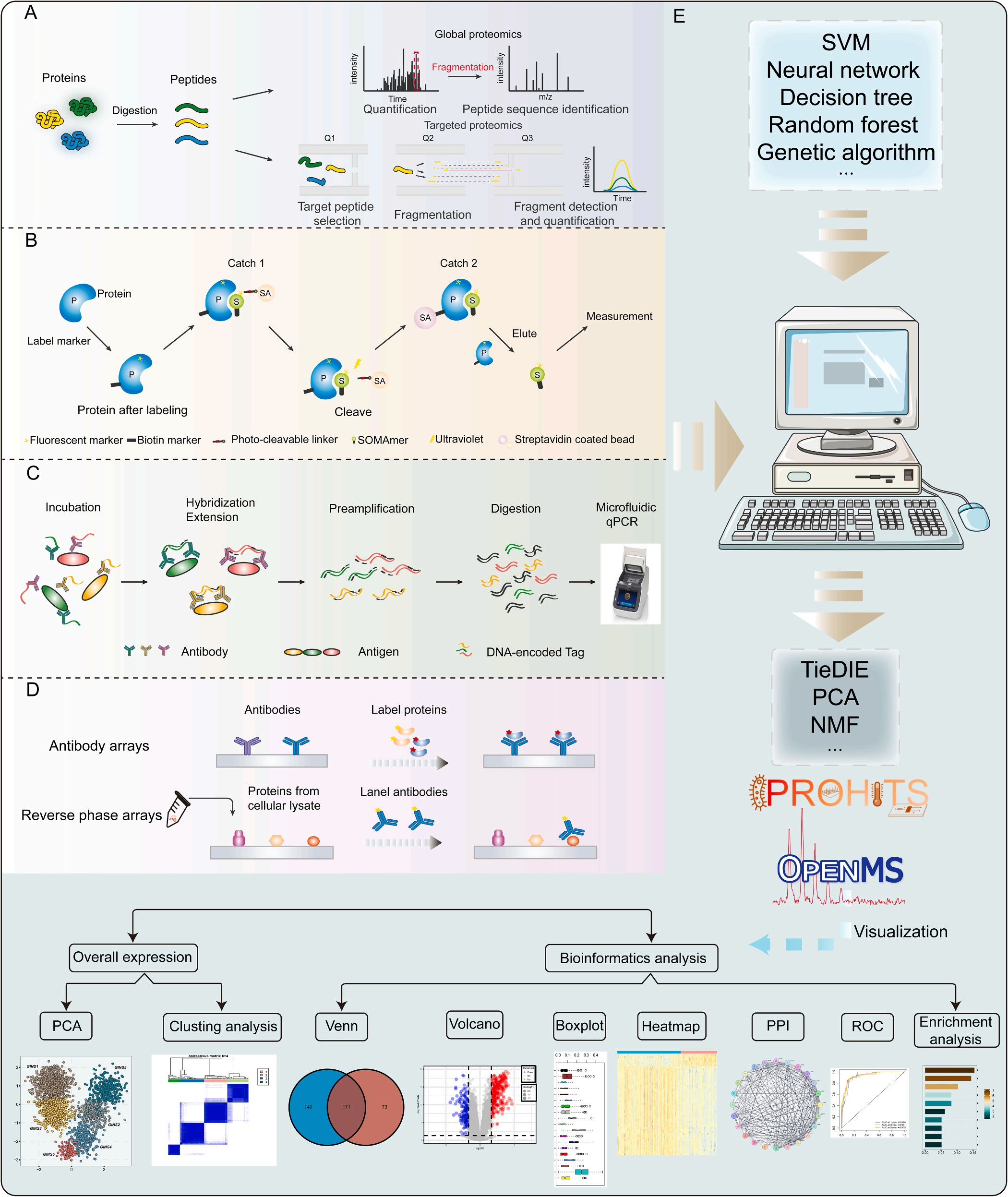
图1. 蛋白质组学技术处理、数据分析和集成。[1]
传统基因组学如同阅读建筑图纸,而蛋白质组学则是实地考察建成的大厦。研究发现,肿瘤组织中蛋白质表达水平与基因测序结果的一致性不足70%,翻译后修饰(PTM)等蛋白质特有变化更是基因检测的盲区。例如,HER2阳性乳腺癌中,约15%的病例存在蛋白质过度表达而基因未突变的特殊类型。
二、临床蛋白质组技术的三大突破
1.高通量质谱技术:新一代Orbitrap质谱仪可同时分析8000+蛋白质,单次检测成本较十年前下降90%
2.动态监测系统:Phospho-specific抗体芯片实现磷酸化修饰的实时追踪
3.AI辅助诊断:DeepOmics系统通过机器学习整合多组学数据,诊断准确率提升至92%
三、精准肿瘤治疗的五大应用场景
- 靶向治疗匹配:PD-L1蛋白表达水平指导免疫治疗应答预测
- 耐药机制解析:EGFR-TKI耐药患者中MET蛋白异常激活占35%
- 微环境监测:CAF特异性蛋白标志物预警肿瘤转移
- 疗效动态评估:治疗4周后凋亡相关蛋白变化早于影像学改变
- 个体化疫苗开发:新抗原肽段筛选效率提升5倍
四、临床转化面临的挑战与对策
当前蛋白质组分析仍存在样本前处理标准化(变异系数>25%)、数据解读专业性要求高等难题。2023年NCI推出的ProCan®计划通过建立万人级肿瘤蛋白质组数据库,使检测结果可比性提升至85%。建议医疗机构采用"三步走"策略:① 重点病种优先突破 ② 建立多学科MDT团队 ③ 开发智能化报告系统
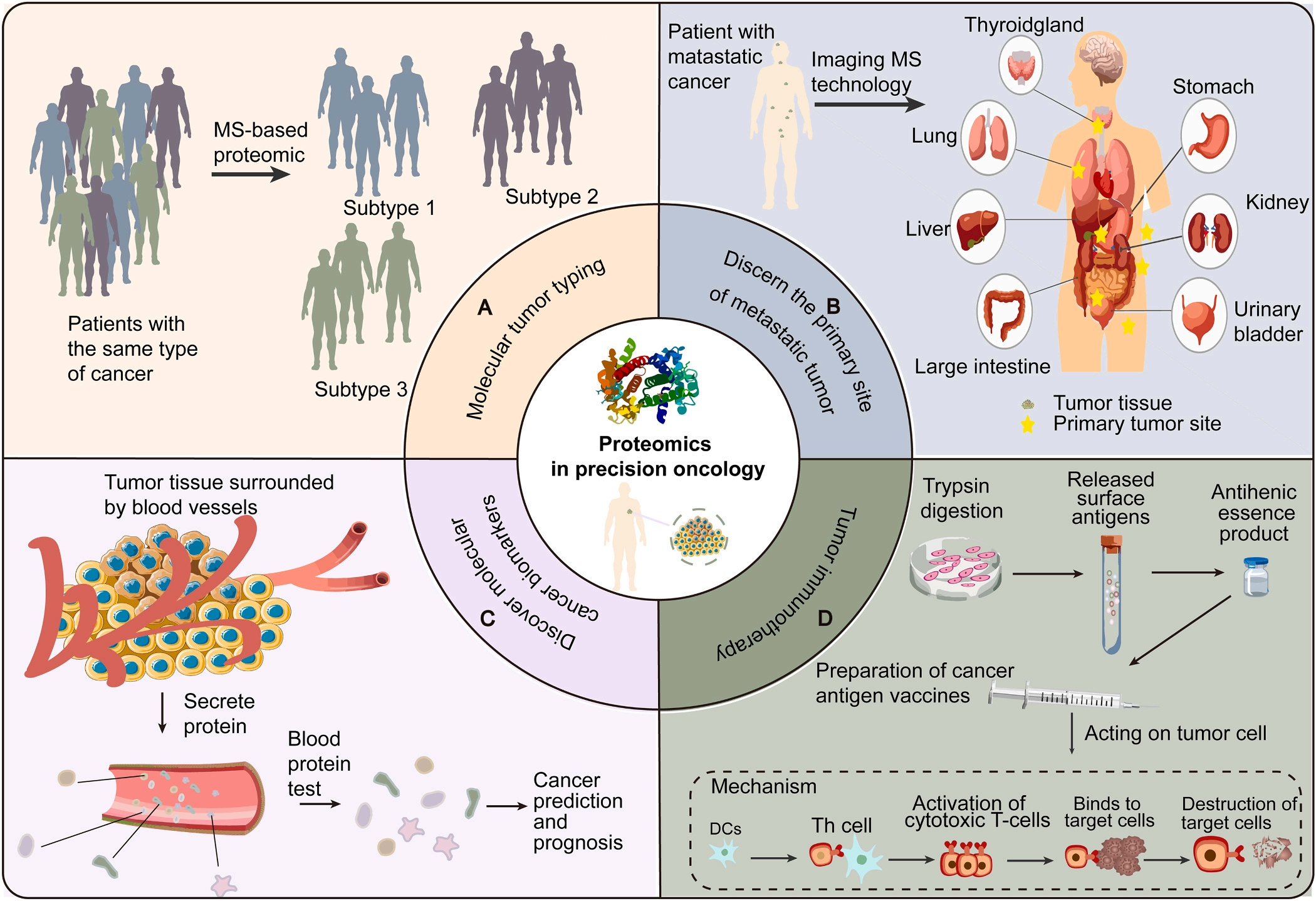
图2. 蛋白质组学助力精准肿瘤学。[1]
五、未来发展方向
随着空间蛋白质组技术(分辨率达1μm)和液体活检蛋白组(灵敏度0.1ng/mL)的突破,2025年有望实现"三个全"目标:全周期监控、全景式分析、全流程自动化。这将对传统肿瘤诊疗模式产生颠覆性革新,真正实现"一人一策"的精准医疗。
参考文献:[1] Z. Zhou, R. Zhang, A. Zhou, J. Lv, S. Chen, H. Zou, G. Zhang, T. Lin, Z. Wang, Y. Zhang, S. Weng, X. Han, Z. Liu, Proteomics appending a complementary dimension to precision oncotherapy, Computational and Structural Biotechnology Journal, 23 (2024) 1725-1739.
科学指南针在全国建立32个办事处和20个自营实验室,拥有价值超2.5亿元的高端仪器。检测项目达4000+项,覆盖材料测试、环境检测、生物服务、行业解决方案、模拟计算等九大业务。累计服务1800+个高校、科研院所及6000+家企业,获得了60万科研工作者的信赖。
免责声明:部分文章整合自网络,因内容庞杂无法联系到全部作者,如有侵权,请联系删除,我们会在第一时间予以答复,万分感谢。











 您已经拒绝加入团体
您已经拒绝加入团体

 2025-05-12
2025-05-12
 4567
4567
 0
0










