【摘要】 本文详细介绍GC-MS技术在血清代谢组学中的优势与应用方法,涵盖极性代谢物提取、衍生化策略、同位素内标使用及数据分析要点,适用于临床与科研场景。
气相色谱-质谱联用技术(GC-MS)已成为代谢组学研究中的重要工具,尤其在血清等复杂生物基质的分析中表现卓越。该技术能够实现对极性与非极性代谢物的高效分离与鉴定,适用于多种生物样本,具备高灵敏度、高稳定性及良好的定量能力,非常符合现代临床实验室对高通量、高精度检测的需求。
为什么选择GC-MS进行代谢组学研究?
在代谢组学研究中,常用的分析平台包括核磁共振(NMR)、液相色谱-质谱(LC-MS)和气相色谱-质谱(GC-MS)。每种技术各有优劣,但GC-MS因其较高的分辨率、较好的重现性以及相对较低的运营成本,在中小分子代谢物鉴定中表现尤为出色。
与1H-NMR相比,GC-MS设备体积较小,无需特殊磁场防护设施,更容易在常规临床环境中部署。而与LC-MS相比,GC-MS在信噪比和数据稳定性方面通常更具优势,有利于构建可靠的代谢物表达模型。
GC-MS的工作机制与优势
在气相色谱-质谱分析过程中,样品中的化合物会依据其物理化学性质在色谱柱中实现分离,并按不同的保留时间依次洗脱。随后,流动相将分离后的组分送入质谱仪,进行离子化并按质荷比(m/z)进一步分离。最终通过保留时间与质谱图的匹配,实现代谢物的定性与定量。
常用的质谱仪包括四极杆和飞行时间质谱仪(TOF-MS)。其中,GC-TOF-MS因具备更快扫描速度和更高分辨率,在高通量代谢组学应用中逐渐成为主流。
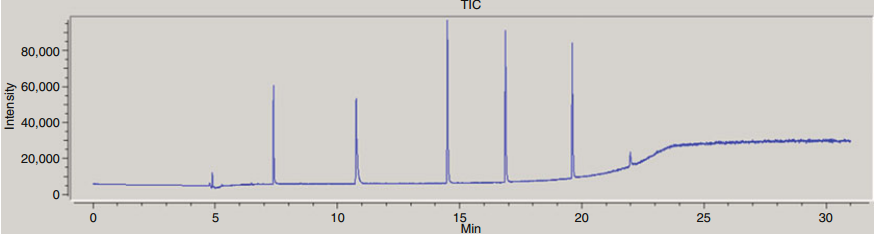
图1. 标准7-烷烃溶液的色谱图,用于保留时间归一化和保留指数的生成。[1]
如何提高GC-MS数据的准确性与重现性?
尽管GC-MS本身是半定量技术,但通过引入内标法,尤其是稳定同位素标记策略(如氘标记代谢物),可显著提高定量准确性。该方法能够有效消除仪器偏差和批次间误差,扩展动态检测范围,并提升低丰度代谢物的检出能力。
此外,合理的实验设计也至关重要。建议在样本序列中插入质量控制样品(QC),并在一开始就设定合适的内标物,以监控整个分析过程的稳定性。
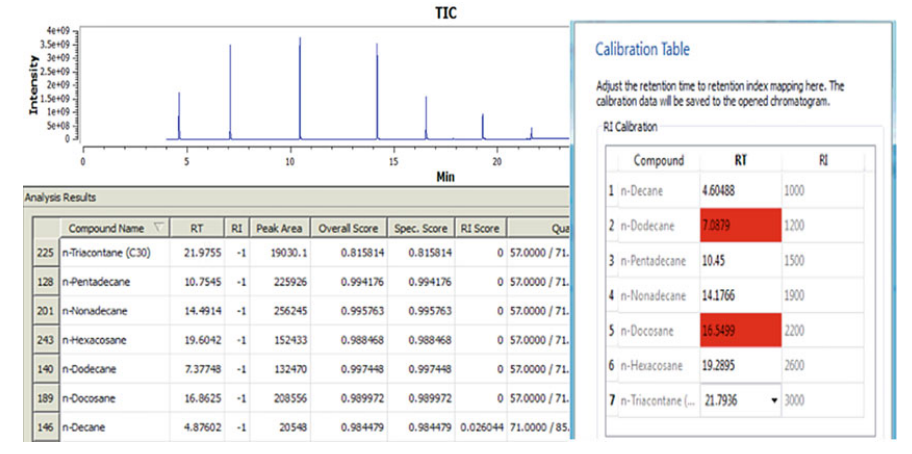
图2. 代谢物检测器中RI标准溶液中七种烷烃化合物的分配程序的截图。[1]
结论
气相色谱-质谱联用技术(GC-MS)在血清代谢组学中兼具高灵敏度、强鲁棒性与良好的临床适用性。通过优化样品前处理、引入内标与质控策略,研究人员能够更准确地识别和定量差异代谢物,从而在疾病生物标志物发现、药理机制研究等领域发挥重要作用。
参考文献:[1] Rattner, J., Farshidfar, F., Bathe, O.F. (2019). Gas Chromatography-Mass Spectrometry and Analysis of the Serum Metabolomic Profile Through Extraction and Derivatization of Polar Metabolites. In: Haznadar, M. (eds) Cancer Metabolism. Methods in Molecular Biology, vol 1928.
科学指南针已获得检验检测机构资质认定证书(CMA)、实验动物使用许可证、“ISO三体系认证”等专业认证,并荣获国家高新技术企业、国家“互联网+科研服务领军企业等多项荣誉。未来,科学指南针将继续朝着“世界级科研服务机构”的目标,在产品研发和用户服务等方面持续努力,为科学发展和技术创新做出更大贡献。
免责声明:部分文章整合自网络,因内容庞杂无法联系到全部作者,如有侵权,请联系删除,我们会在第一时间予以答复,万分感谢。











 您已经拒绝加入团体
您已经拒绝加入团体

 2025-09-11
2025-09-11
 3449
3449
 0
0










