【摘要】 氨是重要的化工原料,同时,由于其高能量密度和可液化的特性,它已被确定为合适的氢载体。

出处:Adv. Mater. 2021, 33, 2008180
背景
氨是重要的化工原料,同时,由于其高能量密度和可液化的特性,它已被确定为合适的氢载体。传统NH3的合成需要高温高压,以及对环境污染严重。
然而,以水为质子提供体,通过光催化还原N2制备NH3被认为是理想的途径。目前光催化NH3产生速率仍然受到其缓慢反应动力学和低效率的阻碍。
研究思路与方案
Han课题组报道了一种简单的自下而上的方法,使用层状Ti3SiC2 MAX作为特定的前体来生产具有高浓度Ti3+物种的C掺杂锐钛矿TiO2纳米片(CTiOx)。层状Ti3SiC2用作结构导向模板、掺杂剂C源和Ti源,用于形成多孔C掺杂的TiOx,其随后被用作合成NH3的光催化剂。
注释:TiO2air:表示C4TiOx在600oC,2h小制得;CXTiOx:X表示H2O2TOE(H2O2辅助热氧化蚀刻策略)的时间。
结果与讨论
结构表征:
从图1b制备得到的C4-TiOx展现出多孔片层结构。进一步通过元素mapping分析可以看出,Ti,O,和C在C4-TiOx表面的均匀分布,如图1c所示。
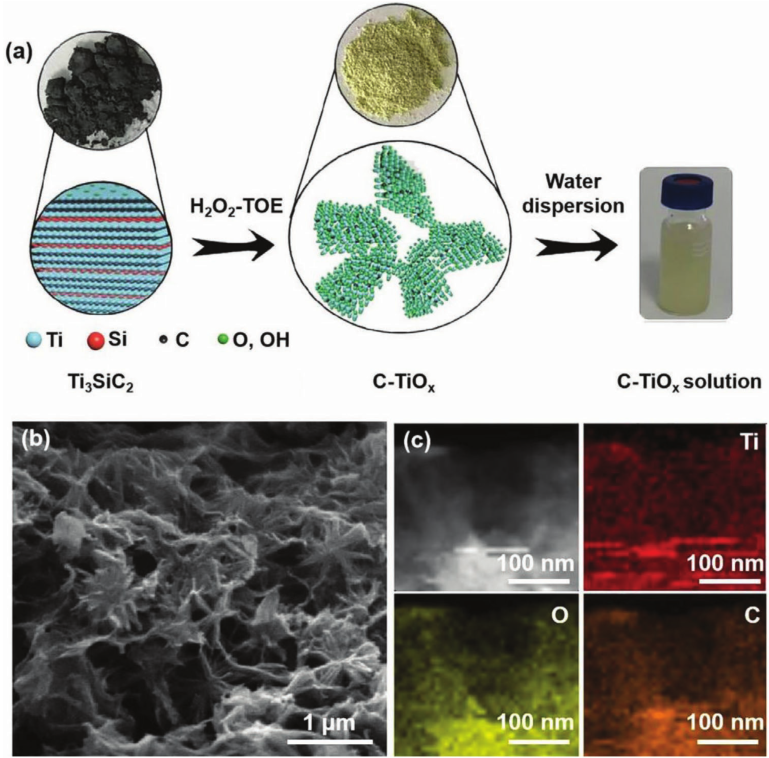
图1(a)C-TiOx的制备示意图,C4-TiOx的结构表征:(b)SEM(c)HAAD-STEM以及对应的元素mapping。
图2a所示,TiO2air表现出得衍射峰与标准卡片为21-1271得锐钛矿一致。其中,C4-TiOx在25.5o处的峰偏移至25.3o,是由于TiO2air中的O被C所取代。C4-TiOx其他的峰与TiO2air一致。
如图2b所示,C4-TiOx的RM峰与TiO2air(星号)基本一致。值得注意的是,在C4-TiOx中存在其他峰(菱形),可归属为Ti-C键的振动。
如图2c所示,俩个主峰归属为TiO2中Ti4+,而在图中可以明显的看出存在Ti3+ 2p3/2和Ti3+ 2p1/2的峰,更重要的是存在俩个Ti2+的峰,证明了存在Ti-C键。
Ti K-边XANES分析的结果(图2d)表明,Ti在C4-TiOx中的边缘能量明显高于在Ti3SiC2中的边缘能量,这表明,C4-TiOx中的Ti原子被成功氧化。
C4-TiOx的XANES轮廓形状与锐钛矿型TiO2的轮廓形状一致,这进一步证实了锐钛矿型TiO2的形成。C4-TiOx的吸收边能略低于TiO2,表明Ti4+物种的平均氧化态降低。
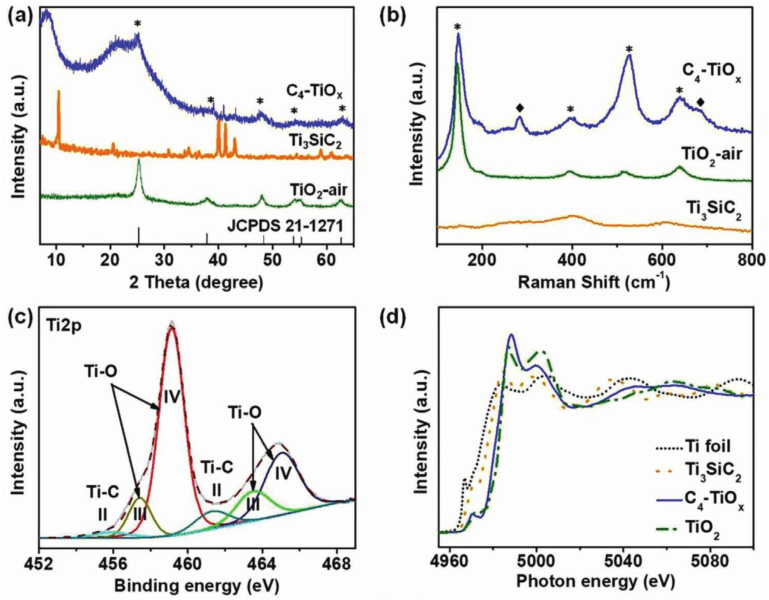
图2(a)XRD,(b)RM,(c)C4-TiOx中的Ti的高分辨XPS,(d)Ti K边XANES光谱。
光电化学测试:
如图3a所示,在低温下只有C4-TiOx具有明显的峰(g=2.083),这是由于Ti3+捕获了电子产生的信号,在光催化过程中能够有效分离光生载流子。
g=2.016时的EPR信号归因于与氧中心自由基(如O-)相关的表面俘获空穴,其可与水或羟基离子反应形成羟基自由基。此外,如图3b所示,C4-TiOx的荧光强度也明显减弱,证明了光生载流子复合得到明显的抑制。
C4-TiOx的荧光寿命也增加到了6.55 ns,明显长于TiO2air(0.53 ns)。图3d所示,不同比例的Ru作为助催化剂,可以看出在负载量为5%时,能够表现出最佳的光催化NH3的产生。
C4-TiOx呈现极高的N2化学吸附峰,这强烈表明C掺杂的TiO2导致N2吸附活性位点的数量显著增加。当没有光或暴露在没有N2或水的光下时,可以产生稀少的NH3,如图3f中的对照实验所示,这表明NH3是通过光驱动的N2还原合成的。
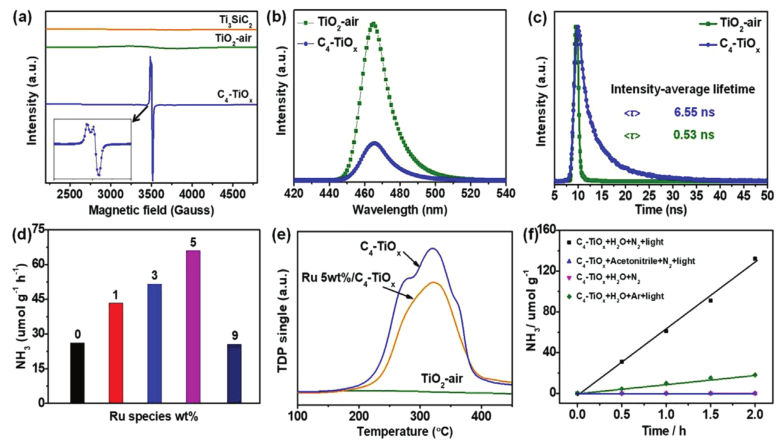
图3(a)在光激发下的低温EPR,(b)PL光谱,(c)时间分辨PL光谱,(d)光催化NH3的产率,
(e)N2的程序升温解吸(TPD),(d)控制实验和光催化NH3产生。
从图4a可以看出,Ti3SiC2和TiO2air的光催化活性相当低,而所有的CTiOx都能够表现出明显的光催化NH3的产率,其中C4TiOx的光催化活性最佳,可达109.3 µmol g-1 h-1。
其次,从图4b可以发现,光催化产生NH3与Ti3+的浓度具有很好的线性关系。C4TiOx的光催化活性活性其吸收范围表现出明显的不同,如图4c,在循环8小时以后仍然具有较高的NH3的生成量。
当使用15N2作为氮源时,产物中15N:14N的丰度比明显高于使用14N2作为氮源时的丰度比,这表明N2气体是光催化合成NH3的来源(图4d)。

图4(a)5%Ru负载不同催化剂的光催化NH3产率,(b)Ti3+浓度与NH3产量的关系,(c)5%Ru-C4-TiOx的吸收光谱与NH3的产量以及插图对应的循环稳定性测试,(d)同位素测量:通过分别与14N2和15N2反应获得的溶液中靛酚的质谱。
本文所有内容文字、图片和音视频资料,版权均属科学指南针网站所有,任何媒体、网站或个人未经本网协议授权不得以链接、转贴、截图等任何方式转载。











 您已经拒绝加入团体
您已经拒绝加入团体

 2021-08-26
2021-08-26
 8839
8839
 0
0










