【摘要】 本文解析传统敷料在动物模型中的临床前局限(如感染率升3倍、愈合延迟40%),并揭示新型水凝胶的四大优势:自愈抗菌(99% MRSA清除率)、智能响应(温敏/pH敏感)、生长因子缓释(再上皮化速率+50%)及葡萄糖调控机制。结合高分研究设计逻辑(如多时间点监测、qPCR验证20+因子),展望智能绷带与精准匹配材料的未来趋势。

当糖尿病小鼠的慢性伤口在 14 天内实现 90% 愈合,当 MRSA 感染创面的细菌被精准清除且新生血管密度提升 60%—— 这些看似神奇的治愈效果,背后是材料科学与生物测试的深度融合。在伤口愈合领域,新型材料正通过动物模型的严格验证,一步步改写传统治疗的局限。
一、 传统敷料的临床前困局
纱布、薄膜、水胶体等传统敷料的短板,在动物实验中被放大呈现:对小鼠全层皮肤缺损模型的对比研究显示,纱布敷料因频繁更换导致的二次损伤,使伤口愈合周期延长 40%;薄膜敷料在感染创面模型中,因透气性差导致厌氧菌滋生率提升 3 倍;水胶体则在高渗液伤口模型中因吸收力不足,出现周围皮肤浸渍的概率高达 65%。这些在动物模型中量化呈现的痛点,正是材料创新的起点。
二、水凝胶的逆袭:四大核心优势改写规则
新型水凝胶在动物实验中的表现令人瞩目。具有双重动态键的抗菌导电水凝胶,在大鼠感染伤口模型中展现出 "自愈 + 抗菌" 双重能力 —— 不仅能在受损后 30 秒内自修复,还通过光热效应实现 99% 的 MRSA 清除率,且经 HE 染色证实无皮肤刺激。更值得关注的是其智能响应特性:在体温下自动成胶的温敏型水凝胶,在兔耳缺损模型中贴合度达 100%,解决了传统敷料易脱落的难题。
而对糖尿病小鼠模型的研究更凸显材料的精准调控能力。双生长因子功能化丝胶水凝胶通过缓释 PDGF 和 EGF,使慢性伤口的再上皮化速率提升 50%,Masson 染色显示其胶原沉积量是对照组的 2.3 倍。而鸟苷四联体水凝胶通过消耗内源性葡萄糖的机制,在高血糖环境中仍能维持稳定的愈合效率,为糖尿病伤口治疗提供新思路。
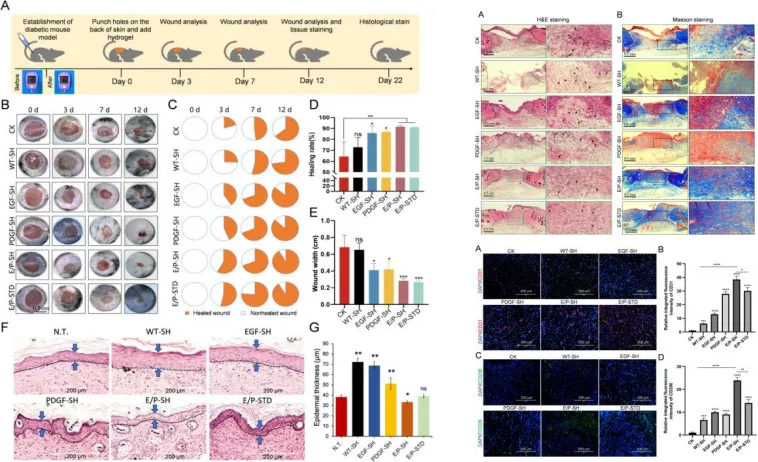
DOI:10.1016/j.bioactmat.2025.06.017
三、高分研究的密码:藏在细节里的测试逻辑
顶级期刊文献揭示,优质材料研究的动物实验设计暗藏玄机。《Bioactive Materials》(IF 18.0)发表的研究中,研究者对伤口进行 0、3、7、10、14 天的多时间点监测,采用 CD31 标记血管、α-SMA 标记肌成纤维细胞,通过图像分析软件量化每一个指标。这种从宏观愈合率到微观分子机制的全链条测试,让材料的作用机理无所遁形。
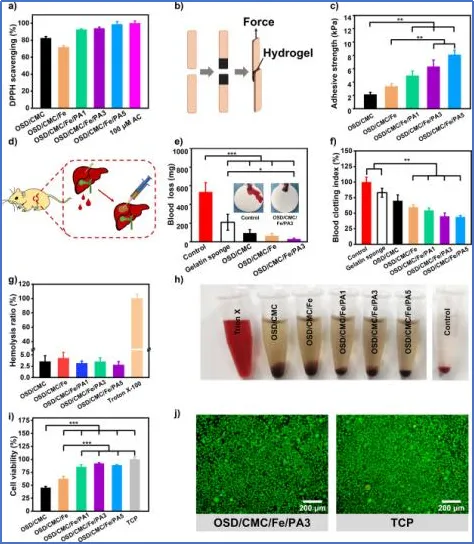
DOI: 10.1016/j.bioactmat.2023.07.015
对比高分与低分研究可见:前者每组至少 8 只动物,进行 3 次独立重复实验,通过 qPCR 检测 TNF-α、VEGF 等 20 余种因子;后者往往仅监测 0、7、14 天三个时间点,仅做 HE 染色便得出结论。从高分SCI的研究路径可见,完善的测试体系能让材料的优势更突出 。
四、未来已来:材料正在变得 "更懂伤口"
智能响应型材料正成为新趋势。pH 敏感水凝胶在感染创面(pH 升高时)自动释放抗菌剂,在小鼠模型中使炎症消退时间缩短 50%;温敏型水凝胶在体温下快速成胶,解决了关节等活动部位的敷料固定难题。更前沿的探索已延伸至 "材料 + 传感器" 领域,可实时监测伤口温度、pH 值的智能绷带,在猪烧伤模型中实现了感染预警与治疗的同步进行。
不同伤口需要精准匹配材料:感染伤口优先选抗菌响应型,慢性伤口侧重生长因子缓释,深层伤口适合可注射填充型。科学指南针的数据库显示,针对性选择材料能使愈合效率提升 40%-60%。
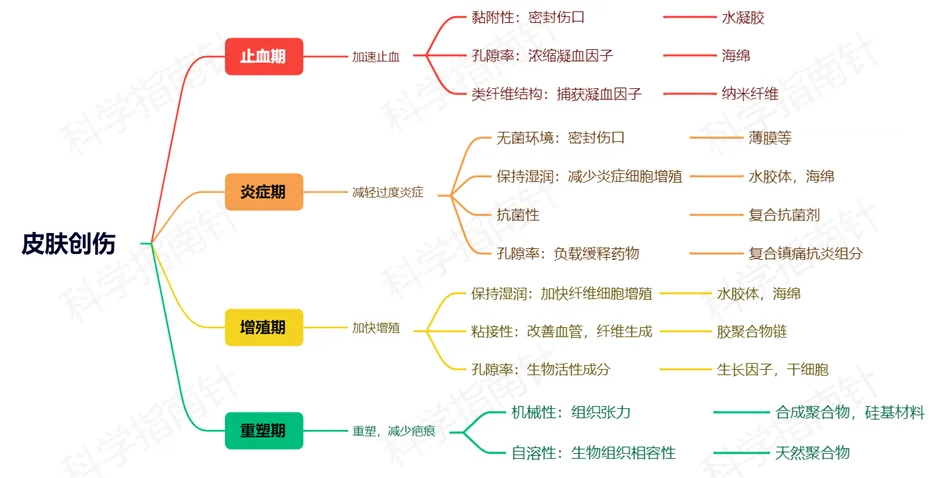
从动物模型中萌芽的材料创新,正在重塑伤口治疗的未来。当水凝胶能像 "智能绷带" 一样感知并响应伤口状态,当每一种材料的效果都有扎实的动物实验数据支撑,伤口愈合将真正进入精准治疗时代。而这一切的起点,始终是那场在实验室里,材料与动物模型的深度对话。
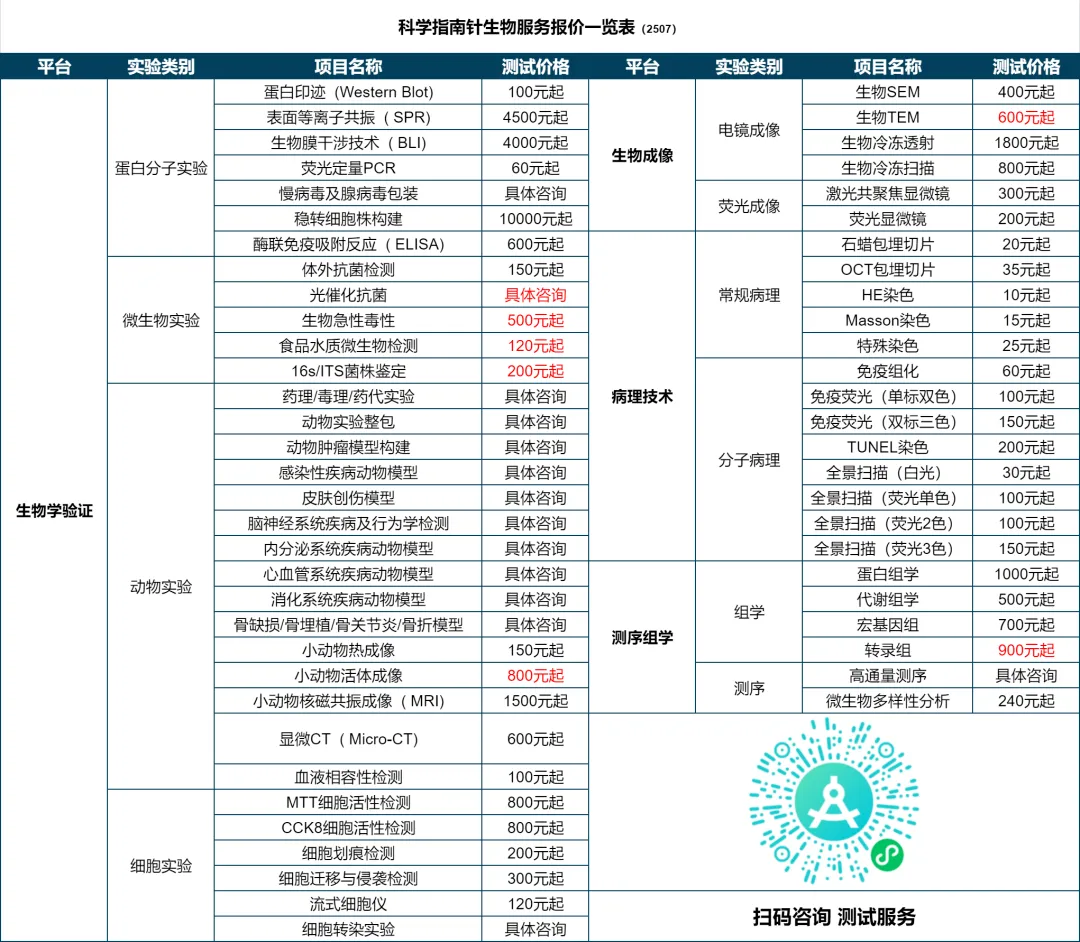
— 扫描表格二维码,即刻咨询测试服务 —











 您已经拒绝加入团体
您已经拒绝加入团体

 2025-08-12
2025-08-12
 3113
3113
 0
0










