【摘要】 近年来,全球锂 (Li+) 需求每年增长6%,由于市场需求快速增长,预计2025年将达到每年95,000吨。

1.研究背景及领域挑战
近年来,全球锂 (Li+) 需求每年增长6%,由于市场需求快速增长,预计2025年将达到每年95,000吨。锂广泛用于可充电锂离子电池、核聚变燃料、储能材料、航天合金、玻璃和陶瓷、医药等材料。含水锂资源约占全球储量的60%,其余为矿床,包括卤水蒸发岩和锂矿石。这些含水锂资源集中在玻利维亚、中国、智利和美国的矿床,比大多数矿石更容易获得。中国最大的碱性盐湖青海湖蕴藏着巨大的锂储量可供开发利用。然而,从盐水中提取锂具有挑战性,因为它们具有不同的化学特性,包括高浓度的Mg2+以及与化学相似的离子共存,特别是K+和Na+。传统技术,包括吸附、沉淀、溶剂萃取、离子交换和电渗析从盐水中分离锂,这些方法受到复杂工艺和预处理要求的限制。这些通常会产生大量废物和高工业规模的生产成本。因此,开发特定的节能技术从高Mg2+/Li+ 比盐水中回收锂是非常有吸引力的。
膜技术具有广泛的水处理潜力,操作简单、环保且能耗低。在膜工艺中,纳滤可以将锂离子与二价离子分离。为了提高膜从各种盐水中提取锂离子的选择性、可扩展性和适用性,膜的合理设计至关重要。通过调整纳米通道结构和化学性质(例如通道形态、层间距和内表面电荷),可以对纳米结构膜进行微调,以从单独的盐水中选择性分离锂离子,从而提高膜性能。
2. 金属有机框架MOF基膜的优势
金属有机框架 (MOF)具有高结晶度、大孔隙率和可调官能团,使其成为定制膜孔结构和化学性质以及针对不同环境应用优化膜性能的潜在材料。近期对用于水溶液中离子选择性传输的MOF膜的研究主要讨论了精心设计的孔系统的设计理念、合成路线、过滤性能和潜在的分离机制。研究了一系列基于MOF的膜(例如 ZIF-8/GO/氧化铝、UiO-66/聚对苯二甲酸乙二醇酯和MOFs/聚氯乙烯混合膜)的金属离子选择性和渗透性。UiO-66具有高可调谐性、优良的水稳定性、简单和商业上可行的合成方法,是最具代表性的用于制备UiO-66基膜(如UiO-66- SO3H、UiO-66-NH2和UiO-66(Zr/Ti)-NH2膜)的MOFs之一,用于高效离子分离。利用对特定离子具有亲和性的客体分子制备离子选择性膜是一种有效的方法。另一种高度可调的MOF-on-MOF结构策略已被提出,以创建具有埃尺度的不对称孔的膜,以增强一价离子分离。这些发现开发了多种MOF基膜,具有量身定制的亚纳米孔系统,用于离子分离应用。尽管这些用于Li+分离的杂交膜很有前途,但仍有几个挑战需要解决: (1)许多聚合物膜的渗透性和选择性差,(2)聚合物老化,(3) MOF对基质的附着力差,以及MOF在MOF基膜中的分散。(4)缺乏对特定盐水中Li+在膜纳米通道中的转运行为具体理解。为了解决这些问题,MOF-on-MOF膜设计是一个重要的研究方向,该膜具有量身定制的孔隙形态和表面电荷,同时提高了盐水中Li+的分离性能。
3. 文章详情
基于上述难题,我们报道了一种新型的MOF-on-MOF膜(UiO-66- (COOH)2/UiO-66- NH2膜),由双金属离子和不同配体通过种子原位生长构建。通过用其他官能团(-(COOH)2和-NH2)修饰双层UiO-66基膜的介质层,可以调整Li+的选择性。不同表面电荷极性、不同进料浓度和不同驱动力(如浓度驱动或电驱动)的膜纳米通道中Li+的传输行为以及Li+提取的潜在机制也将被系统地研究和阐明。这是首次研究UiO-66-(COOH)2/UiO-66-NH2阳极氧化氧化铝(AAO)膜从代表性的台吉耳卤水(中国青海盐湖)中提取低浓度的Li+。本文首次采用UiO-66-(COOH)2/UiO-66- NH2阳极氧化铝(AAO)膜从具有较高Mg2+/Li+摩尔比的代表性台吉耳卤水(中国青海盐湖)中提取低浓度的Li+。我们的发现将启发基于MOF的膜设计,优化离子选择性膜结构和功能,探索未来工业生产中锂提取的通用指导方针,并有助于促进循环经济。
4. 图文解析
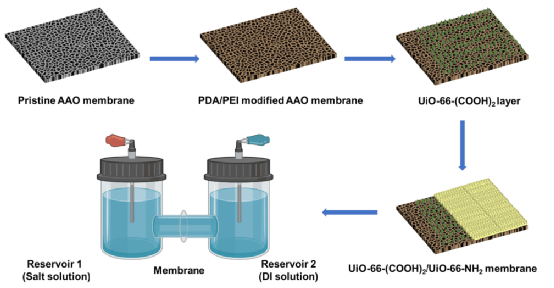
图1. 膜制备和离子转移试验示意图。UiO-66- NH2层是在具有相同锆节点的UiO-66-(COOH)2种子层上合成的。利用离子强度为0.01 M的氯盐溶液(如LiCl、NaCl、KCl、CaCl2和MgCl2)和H电池,利用线性扫描伏安法(LSV)分析了电场驱动的离子在UiO-66-(COOH)2/UiO-66- NH2和UiO-66-NH2膜中的传输。

图2. 原始AAO、PDA-PEI改性AAO、UiO-66-(COOH)2种子层和UiO-66-(COOH)2/UiO-66-NH2膜的SEM图像。用 PDA/PEI 修饰 AAO 膜可以为 MOF 膜的成核和生长提供丰富的儿茶酚和氨基。UiO-66-(COOH)2 在 PDA/PEI 改性膜上的形成导致基板上出现小的种子状颗粒。随后生长的 UiO-66-NH2 与 UiO-66-(COOH)2 种子层具有相同的 Zr 金属节点,在膜上形成了连续的薄膜。
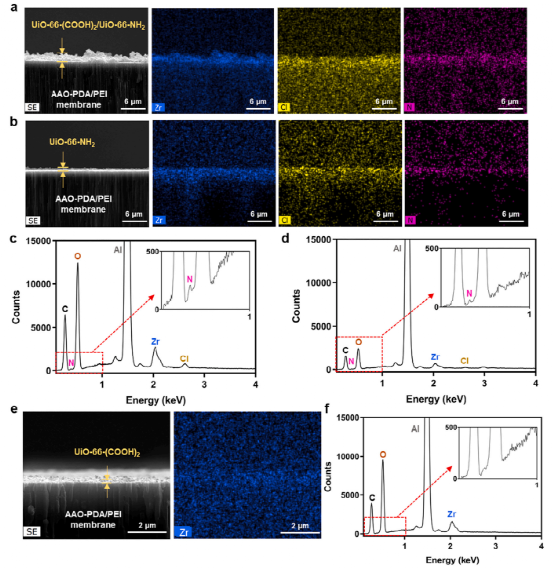
图3. 横截面图像和 EDS 图显示了 UiO-66-(COOH)2/UiO-66-NH2 薄膜中的 Zr、Cl 和 N 元素以及相应的 EDS 光谱;(b, d) UiO-66-NH2 膜的 EDS 横截面图像、Zr、Cl 和 N 的元素图以及 EDS 光谱;(e, f) UiO-66-(COOH)2种子层的EDS截面图、Zr元素图和EDS光谱。UiO-66-(COOH)2/UiO-66-NH2 和 UiO-66-NH2 膜的横截面的 EDS 映射显示 Zr、Cl 和 N在 UiO-66-(COOH)2/UiO-66-和 UiO-66-NH2 薄膜中。所有三个样品都含有 Zr,但 UiO-66-(COOH)2 膜中不存在 N 和 Cl。这表明 N 和 Cl 来自 UiO-66-NH2 层。氮可以通过在 UiO-66-NH2 的 2-氨基对苯二甲酸酯配体中存在 -NH2 来解释。
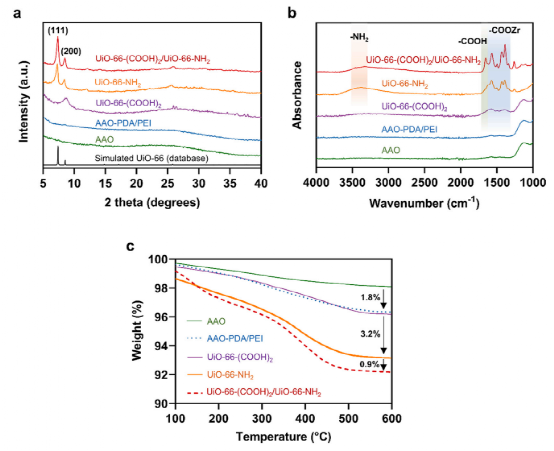
图4. (a) AAO、PDA-PEI 改性 AAO、UiO-66-(COOH)2、UiO-66-NH2 和 UiO-66-(COOH)2/UiO-66-NH2 膜的 X 射线衍射图,以及UiO-66 的模拟峰(参考 ID:02-002-6797);(b) 通过 FTIR 对 AAO、PDA-PEI 改性 AAO、UiO-66-(COOH)2、UiO-66-NH2 和 UiO-66-(COOH)2/UiO-66-NH2 膜进行表面化学分析;(c) TGA 分析显示 AAO、PDA-PEI 改性 AAO、UiO-66-(COOH)2、UiO-66-NH2 和 UiO-66-(COOH)2/UiO-66-NH2 膜的降解和分解。
X射线衍射表明UiO-66-(COOH)2晶种层具有无序结构,在8.6°处有一个宽峰。UiO-66-NH2 膜在 7.3° 和 8.4° 处显示出两个不同的峰,分别符合 (111) 和 (200) 平面。合成的UiO- 66-(COOH)2膜在1300-1700 cm−1处显示较宽的吸收带,与配体的羧酸拉伸和游离羧酸C-O拉伸相对应。这些峰的弱强度是由无定形 UiO-66-(COOH)2 生长的初级阶段引起的。另一方面,由于 2-氨基对苯二甲酸酯配体中胺官能团的振动峰,UiO-66-NH2 膜在 3300-3500 cm-1 处显示出宽吸收带。UiO-66-(COOH)2/UiO-66-NH2膜上也出现了氨基官能团的峰,说明在UiO-66-(COOH)上成功形成了UiO-66-NH2层2层。此外,杂化膜在 1655 cm-1 处显示出强吸收峰,对应于游离羧酸。吸收峰归因于 UiO-66-(COOH)2 作为种子层促进膜上连续且无缺陷的 UiO-66-NH2 薄膜以及 UiO-66-NH2 的引入,促进了 UiO- 66-(COOH)2 二次生长。
AAO膜具有良好的热稳定性,从100到600 ◦C加热时相对较小的质量损失2%。在加热至600 ◦C时,与原始AAO膜相比,PDA/PEI改性膜的质量损失进一步增加1.8%,这是由于PDA/PEI分解造成的。UiO- 66-(COOH)2形成的TGA曲线可与PDA/PEI膜-膜相媲美,表明衬底上有一层非常薄的UiO-66-(COOH)2。
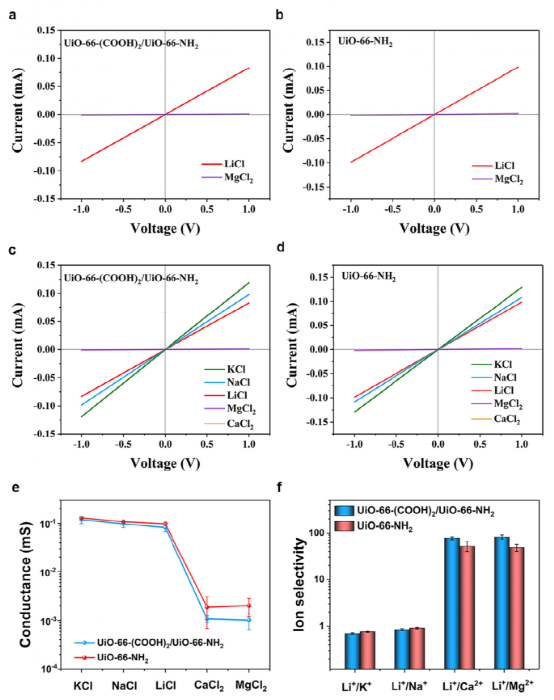
图5. 通过 I-V 测量在 Zr 基膜中的金属离子传输行为。(a) UiO-66-(COOH)2/UiO-66-NH2 膜和 (b) UiO-66-NH2 膜在 LiCl 和 MgCl2 水溶液中的 I-V 曲线;在五种电解质溶液(例如,LiCl、KCl、NaCl、MgCl2、氯化钙);(e) 两种 Zr 基膜的离子电导率和 (f) 金属离子选择性,在 0.01 M 离子强度的五种电解质溶液中测量。
电流-电压 (I-V) 测量在五种电解质溶液(LiCl、KCl、NaCl、MgCl2、CaCl2)中进行,离子强度为 0.01 M,在 -1 至 1 V 范围内,以探索离子传输UiO-66-(COOH)2/UiO-66-NH2 和 UiO-66-NH2 膜的性能。由于双层 UiO-66 膜结构对称,两种膜在所有氯盐水溶液中的 I-V 曲线都是对称的。这表明这些膜对阳离子传输没有优先方向。UiO-66 具有许多三角形窗口孔径 (~6 Å)、四面体空腔 (~8 Å) 和八面体空腔 (~11 Å),提供离子可访问的多尺度纳米通道。
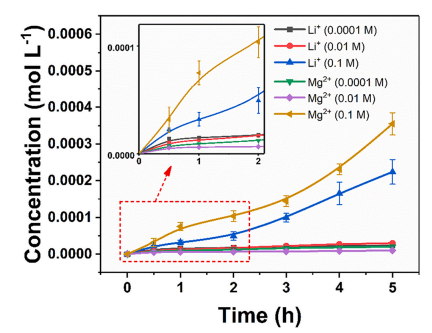
图6. 采用双层 Zr 基膜时,LiCl 和 MgCl2 水溶液的进料浓度在 0.0001 至 0.1 M 范围内时,渗透溶液中的 Li+ 和 Mg2+ 浓度。通过改变浓度进行了 Mg2+/Li+ 选择性对与具有羧基的双层 Zr 基膜(UiO-66-(COOH)2/UiO-66-NH2 膜)的纳米通道相邻的水溶液中进料浓度的依赖性Li+ 和 Mg2+ 的范围从 0.0001 到 0.1 M。离子渗透率与较高浓度的离子进料浓度成正比,但在较低浓度下离子传输行为不同。在 0.0001 M 的低阳离子进料浓度下,膜对 Mg2+ 的静电斥力比对 Li+ 的强。在 0.0001 M 时,Li+ 比 Mg2+ 更容易通过膜,渗透液中 Mg2+/Li+ 摩尔比为 0.873。该比率归因于纳米通道中表面电荷控制的传输行为和较低浓度下的双电层 (EDL) 重叠。
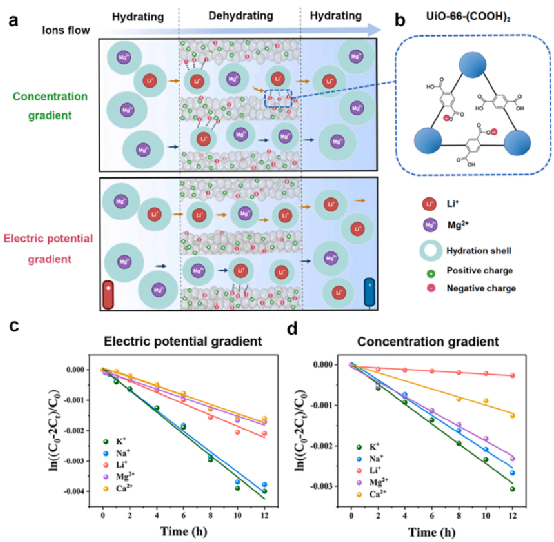
图7. 用于从盐水中提取锂离子的双层 Zr 膜(UiO-66-(COOH)2/UiO-66-NH2 AAO 膜)示意图 (a) 在不同驱动力下和 (b) UiO-的化学结构66-(COOH)2 三角形孔。12 小时内 (c) 电压和 (d) 浓度梯度下 ln((C0-2Ct)/C0) 与时间(进料溶液为合成台金盐水)的关系图。
图 7a 显示了金属离子在这两种驱动力下在合成泰金尔盐水中通过 Zr 基膜与羧基的迁移行为。水溶液中的 Li+ 和 Mg2+ 以水合离子的形式存在,直径分别为 7.64 Å 和 8.56 Å。UiO-66-(COOH)2/UiO-66-NH2-AAO膜的三角窗直径小于6 Å,相对小于Li+和Mg2+离子的水合离子尺寸,但大于它们的离子直径。因此,Li+和Mg2+离子要进入Zr基膜的孔隙结构,它们必须处于部分脱水状态,然后再水化离开孔隙进入水溶液。在外加电压的驱动下,Li+ 在纳米通道内的离子迁移率可能大于 Mg2+,因为部分脱水的 Li+ 壳更紧凑,尺寸比 Mg2+ 更小。相反,Li+在浓度梯度驱动力下的迁移率低于其在电驱动力下的迁移率。Li+ 的渗透很容易被带负电的 -(COOH)2 捕获或吸引,而 Zr4+ 相对于 Mg2+ 的截留率较小。
5.结论
本研究提出了一种通过种子辅助原位生长制备 UiO-66-(COOH)2/UiO-66-NH2 AAO 膜的简便方法,用于从含有高 Mg2+/Li+ 比的合成泰金纳盐水中回收锂。与 UiO-66-NH2 膜相比,具有羧基的双层 UiO-66 基膜在电场驱动过程下对一价离子的选择性高于二价金属离子。经过对进料浓度影响的研究,这种带有羧基的双层膜在进料的相对较高的 Mg2+/Li+ 摩尔比下表现出更好的选择性。在浓度梯度下,由于需要部分脱水的 Li+ 来克服更多的能垒和来自羧基的结合位点,这种膜在合成泰金尔盐水中表现出更好的 Mg2+/Li+ 分离性能。这项研究将激发 MOF-on-MOF 膜制备的未来工作,并为使用节能工艺的人造纳米结构膜从商业或天然盐水资源中增强锂富集提供指导。
文献链接:
https://www.sciencedirect.com/science/article/abs/pii/S0011916422001886











 您已经拒绝加入团体
您已经拒绝加入团体

 2022-05-09
2022-05-09
 8925
8925
 0
0










